헬스케어 분야 '반지의 제왕'은?…웨어러블 기기 대전 돌입
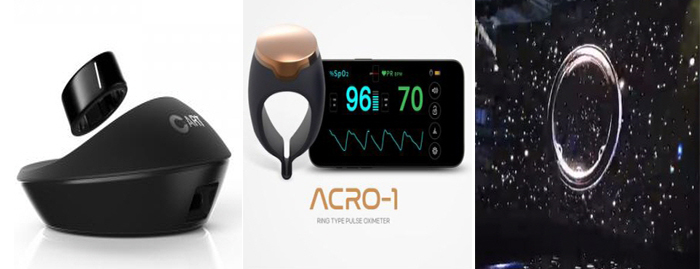
메디칼타임즈=이인복 기자웨어러블 기술이 눈부시게 발전하면서 24시간 착용하며 각종 건강 지표를 모니터링하는 반지형 헬스케어 기기들이 각축전을 벌이고 있다.간단한 착용만으로 심박수나 운동량 측정부터 혈압 등 활력 지수까지 측정이 가능하다는 점에서 스마트워치 등을 대체하는 대항마로 떠오르고 있는 것.12일 의료산업계에 따르면 웨어러블과 센서 기술의 발전으로 얇은 반지 형태의 헬스케어 기기들이 속속 등장하며 새로운 시장을 구축하고 있다.웨어러블 기술의 발전으로 반지형 헬스케어 기기들이 쏟아져 나오고 있다(사진 왼쪽부터 카트 비피, ACRO-1, 갤럭시링)일단 시장 선점에 성공한 것은 바로 스카이랩스다. 반지형태의 혈압계인 카트 비피(CART BP)가 이미 시장에 진출해 임상 현장에서 활용되고 있기 때문이다.특히 카트 비피는 의료기기로 허가를 마친데 이어 현재 가장 정확도가 높은 것으로 알려진 커프를 활용한 혈압 측정에도 밀리지 않는 성능을 보여주면서 임상적 유효성을 입증한 상태다.실제로 카트 비피와 커프형 혈압계를 사용해 양쪽 팔에 3번씩 번갈아 혈압을 측정한 결과 두 측정 방식간 상관 관계는 수축기 0.94, 이완기 0.95로 분석됐다. 비열등성을 인정받은 셈이다.마찬가지로 카트 비피는 24시간 연속혈압측정기는 물론 침습형 동맥혈압측정법 등 현존하는 모든 혈압 측정법과의 비교에서도 비열등성을 입증하고 있다. 사실상 새로운 표준이 되고 있다는 의미다.스카이랩스 이병환 대표는 "표준 혈압 측정법 3가지 모두와 비교해 비열등성을 보여줬다는 점에서 기존 혈압계를 대체할 수 있는 충분한 가능성을 입증했다"며 "이러한 연구 결과를 바탕으로 수가 적용을 준비하고 있으며 올해 내 미국 식품의약국(FDA)와 유럽 CE 인증을 목표로 하고 있다"고 말했다.이처럼 스카이랩스가 반지형 헬스케어 기기의 가능성을 보여주면서 후발주자들도 속속 시장에 도전장을 내밀고 있다.지난해 12월 시장에 나온 올케어러블의 반지형 경피적 혈액 산소포화도 측정 기기 '올케어러블 ACRO-1'이 대표적인 경우다.올케어러블은 이미 산소포화도 측정기인 '펄스옥시미터(Pulse Oximeter)'를 생산하고 있던 의료기기 기업.펄스옥시미터는 빛의 흡광도 차이를 이용해 산소포화도를 측정하는 의료기기로 각광을 받았지만 장시간 착용이 힘들고 활동에 제한이 있는 한계가 있었다.이를 극복하기 위해 이 기술을 반지형태로 구현한 것이 바로 올케어러블 ACRO-1이다.이 기기 또한 서울아산병원병원에서 진행된 확증 임상을 통해 침습적 동맥혈 산소포화도 측정기기와의 비열등성을 입증하며 의료기기로 허가를 받았다.범용 헬스케어 분야에서도 이같은 반지형 제품 출시는 이어지고 있다. 과거 시계 형태의 스마트워치 기술이 반지로 녹아들고 있는 셈이다.이달 출시된 이메디헬스케어의 '바이탈링'이 대표적인 케이스다. 바이탈링은 3.3g의 티타늄 소재로 센서를 통해 각 생체 신호를 24시간 측정해 인공지능으로 분석하는 기능을 갖췄다.기본적으로 체온과 호흡, 활동량, 수면 패턴, 스트레스, 심박수 등이 제공된다.이를 통해 이메디헬스케어는 바이탈링을 통한 치매노인 원격 케어 실증 사업은 물론 항암 환자를 대상으로 하는 건강 모니터링 실증 사업을 진행중에 있다.또한 인공지능 기반의 연속혈압 측정과 비침습적 당뇨 측정 기능을 추가해 의료기기로 허가를 받기 위한 작업도 진행중에 있는 상태다.이메디헬스케어 이언 대표(길병원 신경외과)는 "손가락은 동맥이 있고 피부가 얇아 시계형 등 손목 대비 생체 신호를 더욱 정확하게 측정할 수 있다"며 "고령화 시대에 다양한 건강관리 및 돌봄 수요 솔루션이 될 것"이라고 설명했다.이들과 함께 현재 시장에서 가장 관심을 모으고 있는 제품은 역시 삼성전자가 예고한 '갤럭시링'이다.지난달 갤럭시 언팩 행사에서 삼성전자 노태문 사장이 직접 연내 출시를 공표하면서 시장에 관심을 받고 있는 상황.여기에 다니엘 승 리(Daniel Seung Lee) 삼성전자 B2B 웨어러블·IoT·액세서리 글로벌 총괄이 이달 다시 한번 구체적으로 '하반기'라며 출시를 공식화하면서 이목을 끌고 있는 상태다.아직까지 구체적인 스펙이 공개되지는 않았지만 갤럭시링은 심박수와 혈중 산소포화도는 물론 수면관리, 운동량 측정, 스트레스 관리 등 현존하는 헬스케어 기능이 모두 포함될 것으로 전해지고 있다.이 기술들은 이미 갤러시 워치 등 웨어러블 스마트 워치 등에서 구현되지만 반지 형태로 24시간 모니터링을 한다는 것은 또 다른 차별성이 될 수 있다.일각에서는 비침습형 혈당 관리 기능이나 체온 감지 기능도 언급되고 있지만 아직까지 이에 대한 구체적인 사항은 공개되지 않았다.웨어러블 기기사인 A의료기기 기업 대표는 "이미 애플워치의 등장부터 의료기기와 헬스케어 기기, 웰니스 기기의 구분은 의미가 없어졌다"며 "디자인과 기존 고객의 충성도 등을 고려한다면 갤럭시링의 등장은 웨어러블 업계에 엄청난 파장을 일으킬 수 밖에 없다"고 내다봤다.